南湖新闻网讯(通讯员 崔少婕)近日,我校生物医学与健康学院、生命科学技术学院崔少婕研究员与西南医学中心Jin Ye教授合作,在国际期刊Advanced Science发表题为“Ferroptosis: The Demise of Cells through Phospholipid Peroxidation”的综述论文。该论文系统总结了铁死亡发生的脂质代谢基础,重点阐述了多不饱和磷脂过氧化在铁死亡中的核心作用,并探讨了不同组织对铁死亡敏感性的代谢根源及其潜在干预策略。
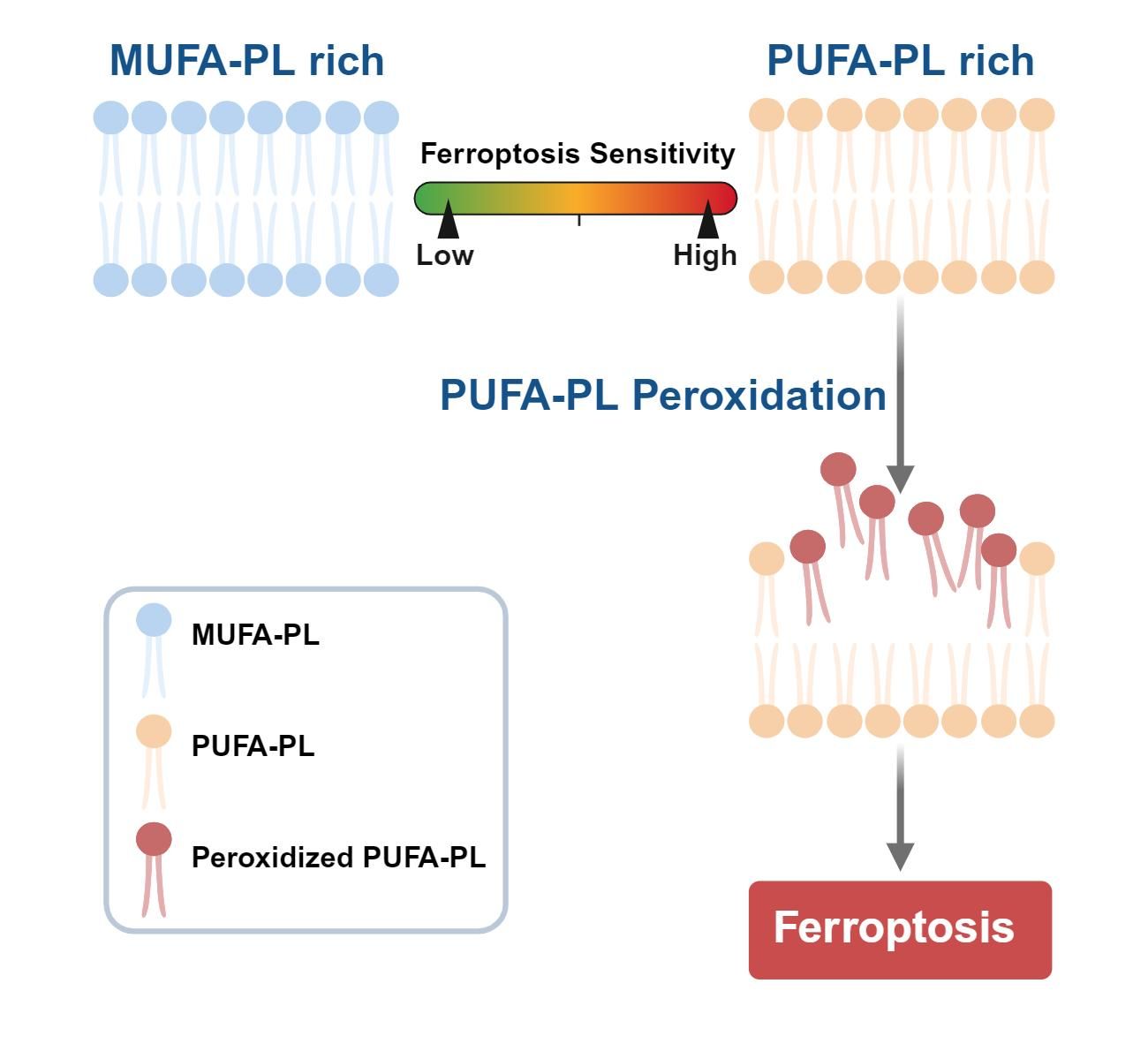
铁死亡是一种由铁依赖性脂质过氧化驱动的调控性细胞死亡方式,其本质并非传统意义上的“蛋白执行程序”,而是一场发生于细胞膜上的氧化失控。该综述指出,细胞对铁死亡的敏感性,很大程度上取决于膜磷脂组成,尤其是多不饱和脂肪酸(PUFA)所构成磷脂的含量、分布及其氧化反应性。文章系统梳理了PUFA磷脂的合成与重塑途径,指出这些代谢过程决定了细胞膜中可被过氧化的底物储备,是影响铁死亡阈值的关键环节;相对地,单不饱和脂肪酸(MUFA)磷脂及脂溶性抗氧化体系则可通过限制磷脂过氧化反应,提升细胞对铁死亡的抵抗能力。
在此基础上,论文进一步从“脂质代谢决定组织铁死亡易感性”的角度,重点讨论了脑、肝脏和睾丸/精子等组织的代表性特点。研究认为,大脑富含DHA、AA等多不饱和磷脂,且氧代谢水平高,因此对脂质过氧化极为敏感;肝脏则因同时承担脂质合成、重塑、摄取、输出及铁代谢等功能,成为铁死亡易于被触发的重要器官;而精子膜富含长链多不饱和脂肪酸,却在成熟过程中逐渐丧失经典GPX4依赖的抗脂质过氧化保护,因此可能处于天然接近铁死亡阈值的特殊状态。上述分析为理解不同组织和疾病背景下铁死亡的发生机制提供了统一的脂质代谢框架。
论文还对铁死亡的转化应用前景进行了讨论。文章指出,尽管近年来铁死亡机制研究取得了快速进展,但其临床转化仍面临关键瓶颈,其中之一是缺乏可用于组织和患者样本检测的可靠标志物。作者结合前期研究,介绍了过氧化PRDX3作为潜在铁死亡标志物的应用价值,强调其有望为体内铁死亡的识别和疾病分型提供新工具。同时,论文提出,体外有效的抗铁死亡策略并不一定能够直接转化为体内治疗获益,未来应遵循“合适时间、合适组织、合适程度”的干预原则,在不影响正常铁依赖生理功能的前提下实现精准调控。
此外,文章还强调了营养干预在铁死亡相关疾病防治中的潜力。由于饮食可直接塑造细胞膜脂质组成,调节PUFA磷脂与MUFA磷脂的相对比例,因此有望成为干预铁死亡的生理性切入口。特别是在肝脏疾病中,以橄榄油为代表、富含油酸的饮食模式,可能通过提升MUFA磷脂、降低多不饱和磷脂过氧化压力而抑制铁死亡,从而对脂肪肝等慢性肝病产生保护作用。这一观点为从膳食和代谢层面干预铁死亡相关疾病提供了新的理论依据。
我校崔少婕研究员为第一作者兼共同通讯作者。团队近期还在经典细胞生物学方法学书系Methods in Cell Biology发表章节“Detecting ferroptotic cells using an antibody against hyperoxidized PRDX3”,系统介绍了利用5H7c抗体检测过氧化PRDX3、从而识别铁死亡细胞和组织的方法学体系。
论文链接:https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202524387
相关章节链接:https://www.sciencedirect.com/science/chapter/bookseries/abs/pii/S0091679X26000828?via%3Dihub
英文摘要:
Ferroptosis is a form of regulated cell death driven by iron-dependent peroxidation of polyunsaturated phospholipids. The susceptibility of cells to ferroptosis is often strongly shaped by lipid metabolic pathways that determine the abundance, distribution, and redox reactivity of polyunsaturated phospholipids. Enzymes that activate and incorporate polyunsaturated fatty acids into phospholipids generate the substrates whose peroxidation causes ferroptosis, thereby sensitizing cells to ferroptosis. In contrast, synthesis of monounsaturated phospholipids and the presence of lipid-soluble antioxidants limit the accumulation of phospholipid peroxides, thereby protecting cells from ferroptosis. Thus, different tissues may display characteristic ferroptotic responses caused by their unique lipid composition and antioxidant capacity. This review summarizes the metabolic foundations that determine the susceptibility of cells to ferroptosis and discusses the possibility of treating human diseases by modulating cellular sensitivity to ferroptosis.
审核人:金安江