南湖新闻网讯(通讯员 付亚楠)近日,动物科学技术学院、动物医学院彭贵青教授团队研究成果在Cell Resports发表了题为“ALG6 orchestrates coronavirus replication via the endoplasmic reticulum stress-autophagy Axis”的研究论文。研究揭示了宿主因子α-1,3-葡萄糖基转移酶(Alpha-1,3-glucosyltransferase,ALG6)是多种冠状病毒复制必需的宿主因子,为冠状病毒的治疗提供一种新的药物靶点。
冠状病毒是对全球公共卫生构成重大威胁的一类病原体。作为一种严格的细胞内寄生微生物,其完整生命周期(包括入侵、复制及释放)高度依赖于对宿主因子的劫持。因此,解析冠状病毒与宿主之间的互作网络,并鉴定关键的依赖性宿主因子,对理解冠状病毒的生命周期及开发抗病毒策略至关重要。然而,目前对冠状病毒-宿主因子互作网络的研究仍处于初级阶段,亟待深入探索和完善。
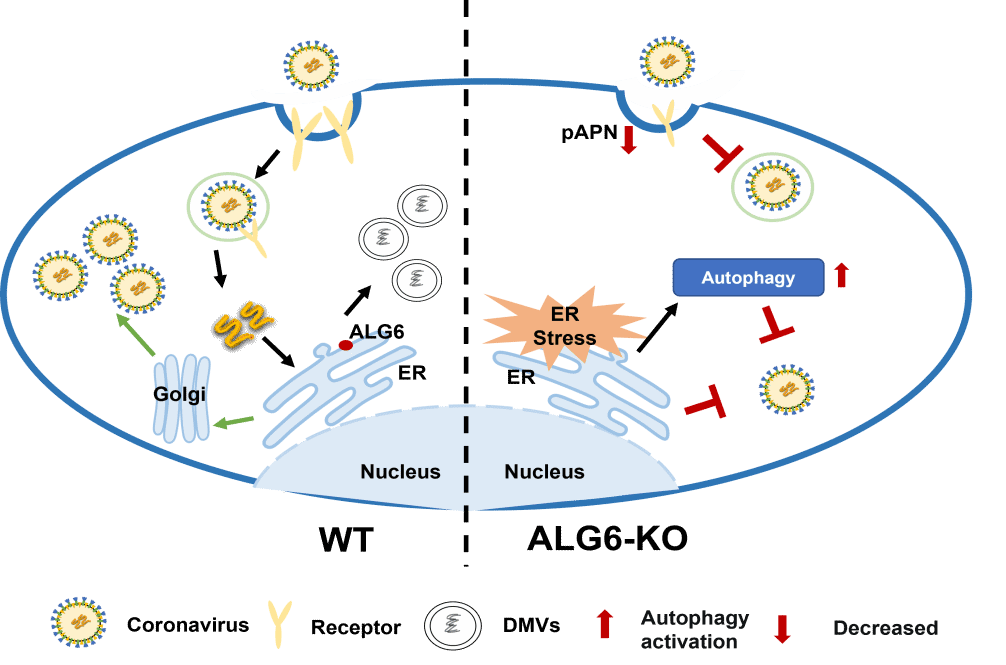
研究发现,宿主因子ALG6能够调控多种冠状病毒的复制。ALG6缺失可从多个层面抑制病毒复制,证实其催化活性直接决定着病毒的复制效率。敲除ALG6后,病毒入侵所依赖的受体——氨基肽酶N(ANPEP)的表达水平显著下调,从而在病毒进入环节即建立第一道防线。进一步机制研究表明,ALG6缺失会触发宿主细胞内质网应激反应,为病毒复制营造不利的细胞环境。更为关键的是,ALG6缺失主要通过激活内质网应激引发的下游自噬通路,有效阻断病毒复制。透射电子显微镜成像分析显示,敲除ALG6能破坏冠状病毒复制所必需的双层囊泡(DMVs)的形成。DMVs作为病毒在宿主细胞内搭建的“复制工厂”,其形成受阻意味着病毒失去了基因组复制的重要场所。
研究系统性揭示了ALG6是调控冠状病毒复制的关键宿主因子,并阐明了其通过影响病毒入侵、诱发内质网应激与自噬、最终破坏DMVs形成的多重作用机制。这为深入理解冠状病毒复制机制提供了新的视角,并为开发针对宿主因子的广谱抗冠状病毒药物提供了新靶点。
华中农业大学动物科学技术学院、动物医学院博士生付亚楠为论文的第一作者,彭贵青教授和谢胜松教授为论文的通讯作者,华中农业大学为通讯作者单位。该研究得到了国家自然科学基金,国家重点研发计划项目的资助。
论文链接:https://www.cell.com/cell-reports/fulltext/S2211-1247(26)00186-5
英文摘要:
Coronaviruses (CoVs) constitute a major global health threat, and their replication is inseparable from host factors. Investigating host-virus interactions is critical for elucidating the coronavirus life cycle. Here, we identify Alpha-1,3-glucosyltransferase (ALG6) as an essential host factor for CoV replication. Mechanistically, its catalytic activity governs TGEV replication, and ALG6 knockout (KO) inhibits viral entry by downregulating the receptor aminopeptidase N (ANPEP). Moreover, our results indicate that ALG6 KO triggers endoplasmic reticulum (ER) stress, resulting in suppressed viral replication. Further investigations demonstrate that ALG6 KO predominantly hinders viral replication by triggering downstream autophagy induced by ER stress. Transmission electron microscopy (TEM) analysis reveals that ALG6 KO disrupts the formation of double-membrane vesicles (DMVs) during the initial stages of viral replication. In summary, our findings underscore the crucial role of ALG6 in the replication of CoVs, presenting a promising avenue for the development of potential therapeutic strategies against future coronavirus infections.
审核人:彭贵青