南湖新闻网讯(通讯员 生医)近日,生物医学与健康学院、食品科学技术学院李锦铨教授团队在Nature Communications期刊上发表题为“In situ gut microbiota editing: Enhancing therapeutic efficacy for bacterial colitis by compatible oral hydrogel microspheres with phages”的研究论文,提出了肠道菌群精准编辑维持肠道稳态新思路。
在肠道这一庞大的“微生物生态系统”中,肠道菌群在维持机体健康方面发挥着至关重要的作用。其不仅参与食物的消化与营养吸收,还与机体的免疫调控、神经活动及情绪状态密切相关。然而,当病原菌入侵或肠道菌群结构发生失衡时,肠道稳态将被破坏,从而引发腹泻、肠道炎症及代谢紊乱等多种疾病。传统治疗通常依赖抗生素,但抗生素对肠道微生物群的非选择性杀伤不仅清除了病原菌,也导致共生有益菌的大量损失,进一步加剧菌群失衡,并可能促进耐药细菌的产生与传播。基于此,该团队提出了一种新的治疗思路—肠道菌群精准编辑,旨在通过选择性调控特定菌群组成,实现病原菌的定向清除与肠道微生态的精准重建(图1)。
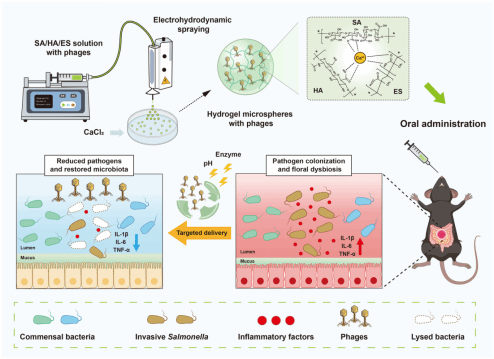
图1 噬菌体微球口服递送平台的构建与肠道菌群原位编辑示意图
噬菌体是一类以细菌为宿主的病毒,具有严格的宿主特异性,仅能感染特定的细菌种类,而对人体细胞及其他非靶向微生物几乎不产生影响。基于这种高度特异性,噬菌体可在不破坏肠道整体微生态结构的前提下,实现对病原菌的精准清除,从而达到真正意义上的定向治疗(图2)。然而,噬菌体的口服给药在应用中仍面临诸多挑战。例如,进入胃肠道后,噬菌体需经受胃酸、胆盐及消化酶等多重不利因素的作用,导致其生物利用度显著降低、体内存活率下降,同时在肠道内滞留时间较短,严重制约了其抗菌活性和治疗效果(图3)。
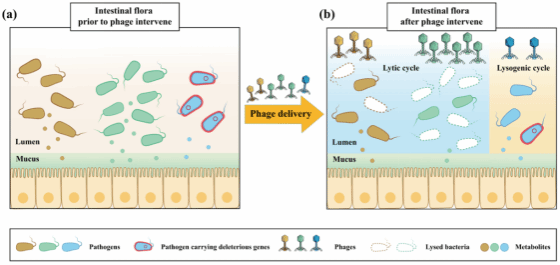
图2 噬菌体口服递送实现肠道菌群原位编辑示意图
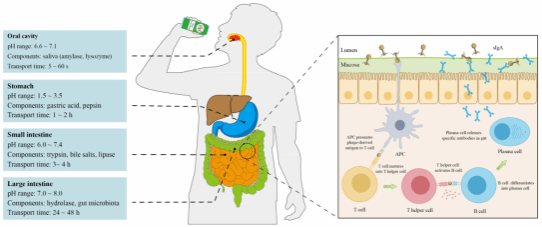
图3 影响噬菌体的体内递送和治疗效果的主要因素
基于此,该团队构建了首个面向“半生命体”(噬菌体)的高效口服递送平台,可精准降低肠道模式病原菌(如沙门氏菌)的数量,并有效避免对肠道益生菌/共生菌的不良影响(图4)。该平台不仅显著增强了噬菌体的体内治疗效果,还实现了肠道菌群的原位精准编辑,兼具“病原菌定向清除”与“共生菌群保护”的双重优势。该项工作为肠道微生态精准调控和噬菌体治疗提供了全新的技术路径,展现出广阔的应用前景和临床转化潜力。
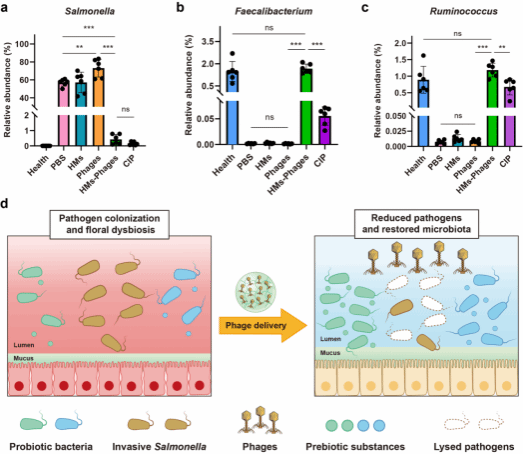
图4 噬菌体微球在小鼠沙门氏菌肠道定植模型中的肠道菌群原位编辑
未来,该平台有望用于精准解析肠道单一细菌的生物学功能及其与健康或疾病的关联。此外,该平台可推广应用于其他肠道菌群失衡相关疾病的治疗,亦可扩展至畜禽养殖以及人群中多重耐药性细菌感染和慢性细菌性炎症疾病的干预,为微生态精准调控及临床治疗提供了新的思路。 该项工作得到国家重点研发计划基金(2023YFD1801000; 2025YFC3408400)、国家自然科学基金(32322082)和华中农业大学校自主创新基金(2662025SPPY004)等项目资助。本文第一作者为食品科技学院2021级博士研究生杨宇帆,并列通讯作者为李锦铨教授和化学学院宋智勇副教授。
原文链接: https://www.nature.com/articles/s41467-025-65498-1
审核:李锦铨