南湖新闻网讯(通讯员 徐思杨 张裕铃)近日,我校生命科学技术学院何进课题组联合湖北省肿瘤医院胃肠外科(湖北省结直肠癌临床医学研究中心)鲁力团队在Cell Reports在线发表了题为“Intestinal microbiota affects the progression of colorectal cancer by participating in the host intestinal arginine catabolism”的研究论文。该研究首次揭示了肠道微生物群通过参与宿主细胞精氨酸代谢网络,调控结直肠癌微环境中的关键信号通路,从而影响肿瘤进展的新机制。该研究为结直肠癌的预防和治疗提供了新思路。
精氨酸代谢产物在癌症中扮演复杂角色(图1):精氨酸酶(Arginase)催化精氨酸转化为鸟氨酸,进一步生成多胺(如腐胺、亚精胺)。多胺可促进肿瘤细胞增殖,抑制免疫应答,加速癌症进展。一氧化氮(NO)是重要的信号分子,由一氧化氮合酶(Nitric oxide synthase)催化精氨酸产生。低浓度NO可激活免疫细胞杀伤肿瘤,而高浓度NO则通过诱导血管生成、促进DNA损伤和Wnt通路激活,驱动肿瘤恶性进展。
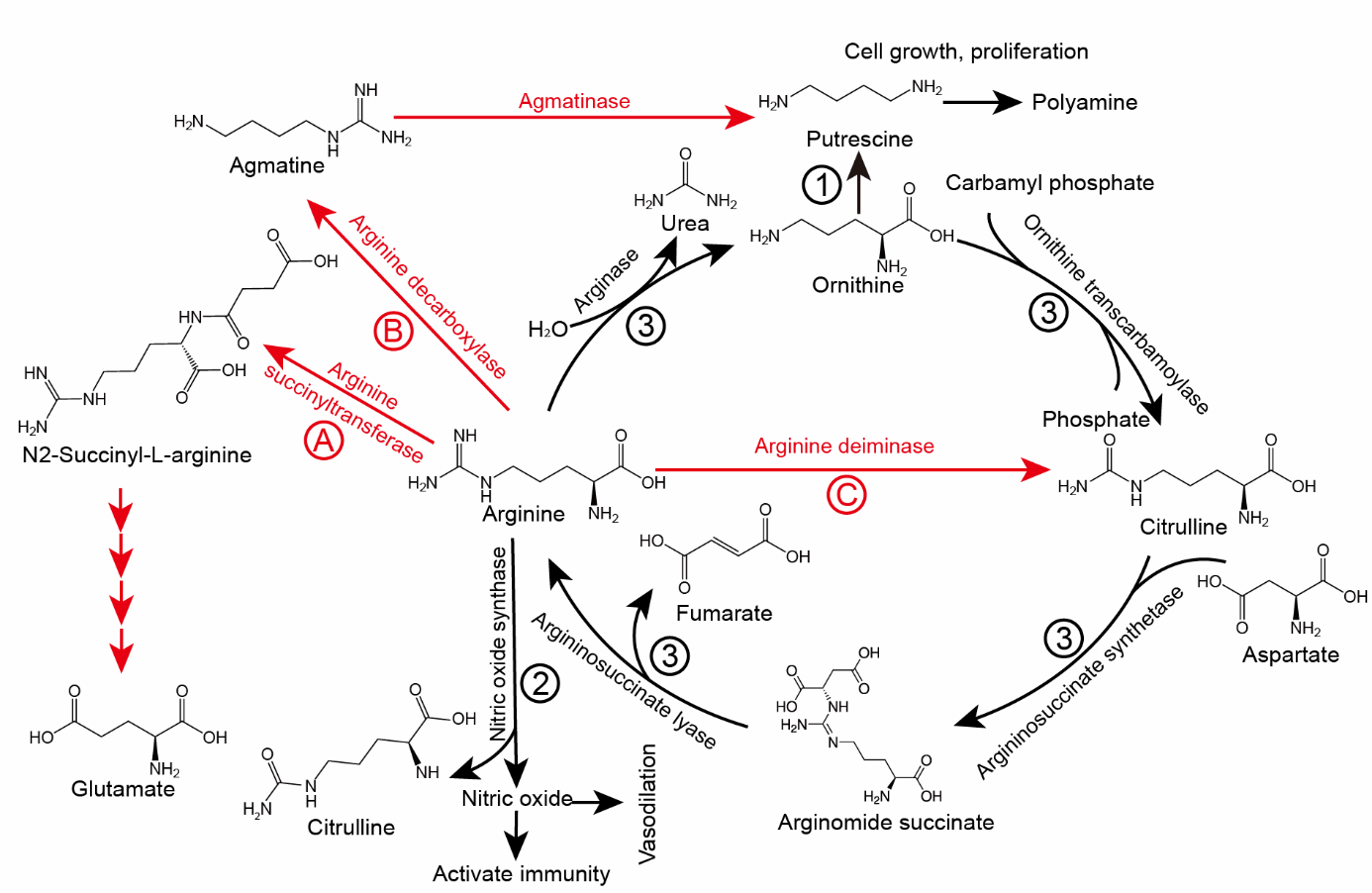
图1. 精氨酸代谢途径影响结直肠癌进展。人体精氨酸分解代谢如下,1. 多胺合成途径: 精氨酸在精氨酸酶的作用下转化为鸟氨酸,后者作为多胺合成的底物,促进细胞生长和增殖。2. 一氧化氮(NO)合成途径:精氨酸在一氧化氮合酶(Nitric oxide synthase)作用下转化为NO。NO可扩张血管,激活肿瘤免疫反应。3. 鸟氨酸循环:在这一途径中,精氨酸不会被消耗,但癌细胞中的部分鸟氨酸循环被阻断。这种结直肠癌细胞需要外源性补充精氨酸才能存活。细菌精氨酸分解代谢如下,A:精氨酸琥珀酰转移酶途径将精氨酸转化为谷氨酸。B:精氨酸脱羧酶将精氨酸转化为γ-氨基嘌呤。C:精氨酸脱氨酶将精氨酸转化为瓜氨酸。
对于癌细胞而言,精氨酸是一把双刃剑:一方面,精氨酸是T细胞等免疫细胞激活的关键底物,精氨酸的存在可增强抗肿瘤免疫,延缓肿瘤进展;另一方面,多数结直肠癌细胞由于鸟氨酸循环缺陷导致无法合成精氨酸,精氨酸的消耗可抑制结直肠癌细胞的生存与增殖。这样就催生了两种截然相反的治疗策略:精氨酸补充疗法与精氨酸剥夺疗法。精氨酸补充疗法是通过向人体补充精氨酸以增强免疫细胞功能,但风险在于精氨酸可能被肿瘤细胞劫持,反而促进肿瘤细胞增殖。精氨酸剥夺疗法则是利用精氨酸降解酶(如精氨酸脱亚胺酶(arginine deiminase))消耗肿瘤微环境中的精氨酸,以抑制“精氨酸营养缺陷型”肿瘤细胞的增殖。
此前研究精氨酸代谢对结直肠的影响均聚焦于人体细胞自身代谢途径上,而忽视了肠道微生物群的作用。本研究发现,肠道微生物群与宿主细胞共同构建了一套完整的精氨酸代谢网络,从临床样本中观察到结直肠癌患者肠道菌群中精氨酸分解代谢显著降低,而肿瘤组织内精氨酸代谢基因(如arg1、nos2)表达异常增强,导致肿瘤微环境中精氨酸浓度失衡。团队结合干湿实验发现,存在于少数细菌(分布在假单胞菌门与芽胞杆菌门的91个细菌种)中的精氨酸琥珀酰转移酶(Arginine succinyltransferase)途径能将精氨酸转化为谷氨酸,直接消耗了微环境中的精氨酸。基于此,研究团队利用基因编辑技术构建精氨酸琥珀酰转移酶缺陷型大肠杆菌Nissle 1917 (ΔacEcN),结合AOM/DSS诱导的小鼠结直肠癌模型,进一步发现抑制肠道微生物群精氨酸琥珀酰转移酶通路可提升结肠内容物中精氨酸水平,激活肿瘤组织内NO合成通路与多胺合成通路,最终通过诱导血管生成、驱动M2巨噬细胞极化及激活Wnt/β-catenin信号通路,加速肿瘤进展(图2)。
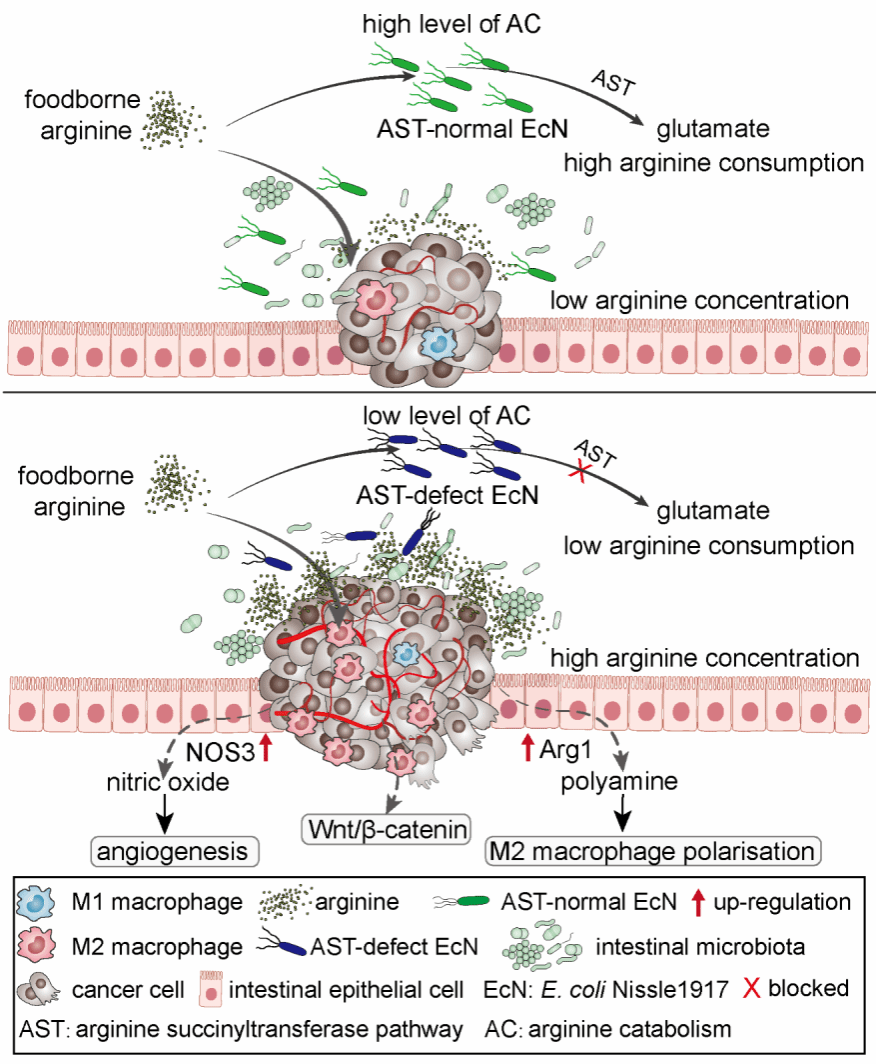
图2. 肠道微生物群通过精氨酸代谢网络调控结直肠癌进程的机制模型:AST缺陷菌株ΔacEcN抑制菌群精氨酸消耗,提升肿瘤微环境精氨酸水平,激活宿主一氧化氮/多胺合成通路,驱动血管生成、免疫抑制及Wnt信号激活。
基于肠道菌群精氨酸琥珀酰转移酶途径与宿主精氨酸代谢网络的相互作用,未来可通过合成生物学策略设计“智能细菌”,在精准剥夺肿瘤微环境中精氨酸的同时为免疫细胞定向递送精氨酸,以破解当前结直肠癌治疗的困境。
生命科学技术学院博士研究生徐思扬为论文第一作者,农业微生物资源发掘与利用全国重点实验室、湖北洪山实验室、我校生命科学技术学院何进教授与湖北省肿瘤医院胃肠外科(湖北省结直肠癌临床医学研究中心)鲁力主任医师为论文共同通讯作者。我校生命科学技术学院博士研究生张裕铃、丁晓琦,硕士研究生杨宜君、高金鸽以及湖北省肿瘤医院放射肿瘤科邹宁副主任医师参与部分研究工作。该研究工作受到国家自然科学基金、湖北省技术创新项目、湖北省肿瘤医院生物医学中心科研项目等的资助。
审核人:何进
论文链接:
https://www.cell.com/cell-reports/fulltext/S2211-1247(25)00141-X